Hukum Kekekalan Massa (Artikel Lengkap)
 Hukum
kekekalan massa atau prinsip kekekalan massa menyatakan bahwa untuk
setiap sistem yang melakukan transfer materi dan energi dalam keadaan
tertutup (keduanya memiliki massa), massa sistem akan tetap konstan
sepanjang waktu, massa sistem tidak dapat mengubah jumlahnya jika tidak
ditambahkan atau dihilangkan. Oleh karena itu, massa kekal dari waktu ke
waktu. Hukum kekekalan massa merupakan bagian dari hukum-hukum dasar kimia.
Hukum ini menjelaskan bahwa massa tidak dapat diciptakan maupun
dimusnahkan, meskipun dapat dirangkai atau dirubah bentuknya. Hukum ini
juga menjelaskan bahwa selama reaksi kimia apapun, reaksi nuklir, atau
peluruhan radioaktif, maka massa total reaktan akan tetap sama dengan
massa produk.
Hukum
kekekalan massa atau prinsip kekekalan massa menyatakan bahwa untuk
setiap sistem yang melakukan transfer materi dan energi dalam keadaan
tertutup (keduanya memiliki massa), massa sistem akan tetap konstan
sepanjang waktu, massa sistem tidak dapat mengubah jumlahnya jika tidak
ditambahkan atau dihilangkan. Oleh karena itu, massa kekal dari waktu ke
waktu. Hukum kekekalan massa merupakan bagian dari hukum-hukum dasar kimia.
Hukum ini menjelaskan bahwa massa tidak dapat diciptakan maupun
dimusnahkan, meskipun dapat dirangkai atau dirubah bentuknya. Hukum ini
juga menjelaskan bahwa selama reaksi kimia apapun, reaksi nuklir, atau
peluruhan radioaktif, maka massa total reaktan akan tetap sama dengan
massa produk.
Hukum kekekalan massa secara luas
digunakan di berbagai bidang seperti kimia, mekanik, dan dinamika
fluida. Secara historis, hukum kekekalan massa ditemukan oleh Antoine
Lavoisier pada akhir abad ke-18. Penemuan beliau adalah penemuan penting
dalam mengubah alkemi menjadi ilmu kimia modern.
Dalam
teori relativitas khusus, massa bukanlah dikonversi menjadi energi,
karena massa dan energi tidak dapat dihancurkan dan energi dalam segala
bentuknya selalu mempertahankan jumlahnya yang setara dengan massa.
Beberapa jenis materi dapat diciptakan atau dihancurkan, tetapi dalam
semua proses ini, energi dan massa tetap tidak berubah, tetapi energi
menjadi berubah bentuk.
1. Sejarah Hukum Kekekalan Massa
Terdapat
falsafat Yunani kuno yang menyatakan bahwa “tidak ada yang datang dari
tidak ada” dan masih berlaku hingga kini. Falsafah ini ditemukan di
Empedokles yang dibuat sekitar tahun 490-430 SM. Selain itu, terdapat
falsafah “sebab ianya mustahil datang dari tidak ada menjadi ada, dan
mustahil juga untuk benar-benar dibinasakan.”
Prinsip
kekekalan massa lebih lanjut dinyatakan oleh Epikurus (341-270 SM) yang
menggambarkan tentang alam semesta, yang bahwa “keseluruhan hal-hal itu
selalu seperti itu sekarang, dan akan selalu seperti itu”.
Filsafat
Jain, yang berdasarkan ajaran-ajaran Mahavira (abad ke-6 SM),
menyatakan bahwa alam semesta dan isinya tidak dapat menghancurkan atau
menciptakan. Teks Jain Tattvarthasutra (abad ke-2) menyatakan bahwa
substansi itu permanen, tetapi mode dapat diciptakan dan dihancurkan.
Prinsip kekekalan massa ini juga dinyatakan oleh Nasir al Din al Tusi
(1201-1274). Dia menyatakan bahwa “tubuh tidak dapat hilang sepenuhnya,
itu hanyalah perubahan bentuk, kondisi, komposisi, warna, dan yang
lainnya dan berubah menjadi hal yang lebih rumit atau kembali ke
dasarnya”.
Hukum kekekalan massa pertama kali
dijelaskan oleh Mikhail Lomonosov (1711-1765). Ia membuktikannya dengan
eksperimen meskipun terkadang ia ditentang. Antoine Lavoisier
(1743-1794) menjelaskan ide-ide ini pada tahun 1774. Dia sering disebut
sebagai bapak kimia modern. Ide-ide yang lainnya sebelum karya Lavoisier
adalah oleh Joseph Black (1728-1799), Henry Cavendish (1731-1810), dan
Jean Rey (1583-1645).
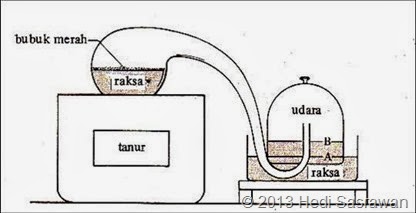 Antoine
Lavoisier mendapatkan hukum ini dengan melakukan eksperimen mereaksikan
cairan merkuri dengan gas oksigen dalam suatu wadah di ruang tertutup
sehingga menghasilkan merkuri oksida yang berwarna merah. Apabila
merkuri oksida dipanaskan kembali, senyawa tersebut akan terurai
menghasilkan sejumlah cairan merkuri dan gas oksigen dengan jumlah yang
sama seperti semula. Dengan bukti dari percobaan ini Lavoisier
merumuskan suatu hukum dasar kimia yaitu Hukum Kekekalan Massa yang
menyatakan bahwa jumlah massa zat sebelum dan sesudah rekasi adalah
sama.
Antoine
Lavoisier mendapatkan hukum ini dengan melakukan eksperimen mereaksikan
cairan merkuri dengan gas oksigen dalam suatu wadah di ruang tertutup
sehingga menghasilkan merkuri oksida yang berwarna merah. Apabila
merkuri oksida dipanaskan kembali, senyawa tersebut akan terurai
menghasilkan sejumlah cairan merkuri dan gas oksigen dengan jumlah yang
sama seperti semula. Dengan bukti dari percobaan ini Lavoisier
merumuskan suatu hukum dasar kimia yaitu Hukum Kekekalan Massa yang
menyatakan bahwa jumlah massa zat sebelum dan sesudah rekasi adalah
sama.
Hukum kekekalan massa tidak terlihat selama
ribuan tahun karena pengaruh berat gas pada atmosfer. Contohnya, kayu
beratnya berkurang setelah dibakar. Ini yang membuat sebagian orang
berpendapat bahwa massanya berkurang, berubah, atau hilang. Namun, jika
kita meneliti di tempat yang tertutup kaca, ditemukan bahwa reaksi kimia
tidak mengubah berat penutup dan isinya. Pompa vakum juga memungkinkan
untuk menimbang berat gas.
Setelah hukum ini
dimengerti, hukum kekekalan massa menjadi penemuan yang sangat penting
dalam yang mengubah alkemi menjadi ilmu kimia modern. Setelah kimiawan
menyadari bahwa bahan kimia tidak bisa hilang tetapi hanya dapat diubah
menjadi zat lain dengan berat sama, para ilmuwan pertama kalinya
melakukan studi perubahan zat.
2. Generalisasi Hukum Kekekalan Massa
Dalam
teori relativitas khusus, kekekalan massa tidak berlaku jika sistem
terbuka dan energi lolos. Namun, itu tetap berlaku untuk sistem yang
benar-benar terisolasi. Jika energi tidak dapat pergi dari sistem, massa
tidak dapat diturunkan. Dalam teori relativitas, asalkan semua jenis
energi masih terperangkap dalam sistem, massanya akan tetap.
Jika
misalnya dicampurkan 32 gram belerang dan 63,5 gram tembaga. Maka
hasilnya adalah tembaga (II) sulfida dengan massa 95,5 gram yang
merupakan massa belerang ditambah massa tembaga.
Perubahan
massa terjadi dimana partikel atom atau partikel lainnya dapat
melarikan diri, tetapi jenis energi lainnya (seperti cahaya atau panas)
diperbolehkan untuk masuk atau keluar. Teori dari seluruh energi dengan
massa dibuat oleh Albert Einstein pada tahun 1905. Namun Max Planck
menunjukkan bahwa perubahan dalam massa sistem sebagai akibat dari
ekstraksi atau penambahan energi kimia (seperti yang dikatakan oleh
teori Einstein) begitu kecil sehingga tidak dapat diukur. Itu adalah
contoh percobaan dari teori Einstein.
3. Penyimpangan Hukum Kekekalan Massa
Penyimpangan
hukum kekekalan massa dapat terjadi pada sistem terbuka dengan proses
yang melibatkan perubahan energi yang sangat signifikan seperti reaksi
nuklir. Salah satu contoh reaksi nuklir yang dapat diamati adalah reaksi
pelepasan energi dalam jumlah besar pada bintang. Hubungan antara massa
dan energi yang berubah dijelaskan oleh Albert Einstein dengan
persamaan E = m.c2. E merupakan jumlah energi yang terlibat, m
merupakan jumlah massa yang terlibat dan c merupakan konstanta
kecepatan cahaya. Namun, perlu diperhatikan bahwa pada sistem tertutup,
karena energi tidak keluar dari sistem, massa dari sistem tidak akan
berubah.
Sumber:
Judul
|
Alamat
|
| 1. Conservation of mass | http://en.wikipedia.org/wiki/Conservation_of_mass |
| 2. Hukum kekekalan massa | http://id.wikipedia.org/wiki/Hukum_kekekalan_massa |
| 3. A. Hukum Kekekalan Massa (Lavoiser) | http://rahmikimia.wordpress.com/kimia-kelas-x/5-hukum-hukum-dasar-kimia/a-hukum-kekekalan-massa-lavoiser/ |
| 4. Hukum-Hukum Dasar Kimia | http://mfyeni.wordpress.com/kelas-x/hukum-hukum-dasar-kimia/ |



Tidak ada komentar:
Posting Komentar